TROPION-Breast03-Studie
Therapie mit Antikörper-Wirkstoff-Verbindung mit oder ohne Immuntherapie bei Patient:innen mit dreifach negativem und frühem Brustkrebs und Tumorrest in der Brust oder Achselhöhle nach neoadjuvanter Chemotherapie und abgeschlossener Operation
Die Rekrutierung der Studie wurde im November 2024 abgeschlossen.
Die TROPION-Breast03 ist eine offene, randomisierte (die Zuordnung der Behandlung für die konkrete Patientin erfolgt per Zufall), kontrollierte, Phase-3 Therapiestudie. In der Studie werden drei unterschiedliche Therapien gegeneinander verglichen und sie richtet sich an Patient:innen mit dreifach negativem (die Tumorzellen haben keine Östrogen-, keine Progesteron- und keine HER2-Rezeptoren.), frühem (Stadium I-III) Brustkrebs. Bei diesen Patient:innen wurde eine medikamentöse Therapie vor der Operation durchgeführt und nach der Operation ein verbliebener Tumor in der Brust und/oder den Lymphknoten der Achselhöhle festgestellt.
Dreifach negativer Brustkrebs ist eine Art von Brustkrebs, bei dem die Tumorzellen an ihrem Zellkern keine Östrogen- oder Progesteronrezeptoren und an ihrer Oberfläche keine HER2-Rezeptoren haben. Eine neoadjuvante Chemotherapie wird vor der geplanten Operation geführt. Nach der neoadjuvanten Chemotherapie werden der Brustkrebs und zusätzlich Lymphknoten aus der Achselhöhle entfernt. Wenn im entfernten Tumorgewebe noch Tumorzellen nachgewiesen werden, ist die Wahrscheinlichkeit hoch, dass noch Tumorzellen im Körper der Patient:in verblieben sind und der Brustkrebs wieder zurückkehrt. Das macht weitere Behandlungen erforderlich.
Was wird in dieser Studie untersucht?
Bei Patient:innen mit dreifach negativem Brustkrebs zeigte der Wirkstoff Datopotamab deruxtecan (Dato-DXd) bereits in einer vorangegangenen Studie Wirksamkeit gegen Brustkrebs. Dato-DXd ist ein Antikörper-Wirkstoff-Konjugat, d. h. ein mit einem Antikörper verbundenes Krebsmedikament. Datopotamab deruxtecan verbindet sich dabei mit einem auf Krebszellen befindlichen Protein namens TROP2 und wird dadurch in die Krebszellen aufgenommen, wo das Krebsmedikament freigesetzt wird und die Krebszellen tötet.
Was ist das Ziel der Studie?
Die TROPION-Breast03 Studie ist geplant für Patient:innen, die nach abgeschlossener medikamentöser, neoadjuvanter Therapie operiert wurden und bei denen trotz der Behandlung ein Resttumor nachgewiesen wurde (in der Brust oder den Lymphknoten der Achselhöhle). Patient:innen mit Resttumor haben in der Regel ein höheres Risiko für ein Wiederauftreten der Krankheit. Die Studie untersucht, ob eine Behandlung mit Dato-DXd in Kombination mit dem Immuntherapeutikum Durvalumab einen Vorteil gegenüber der aktuellen, wirksamen Standardbehandlung (Therapiewahl durch behandelnde Ärzte) hat.
Aktuell liegen keine Informationen vor, ob alle drei Behandlungen gleich wirksam sind oder ob eine der Behandlungen wirksamer ist als die anderen. Um diese Unsicherheit zu beseitigen und in Zukunft die Patient:innen die wirksamste Behandlung geben zu können, werden Studien wie diese TROPION-Breast03 Studie durchgeführt.
Wie ist der Ablauf der Studie?
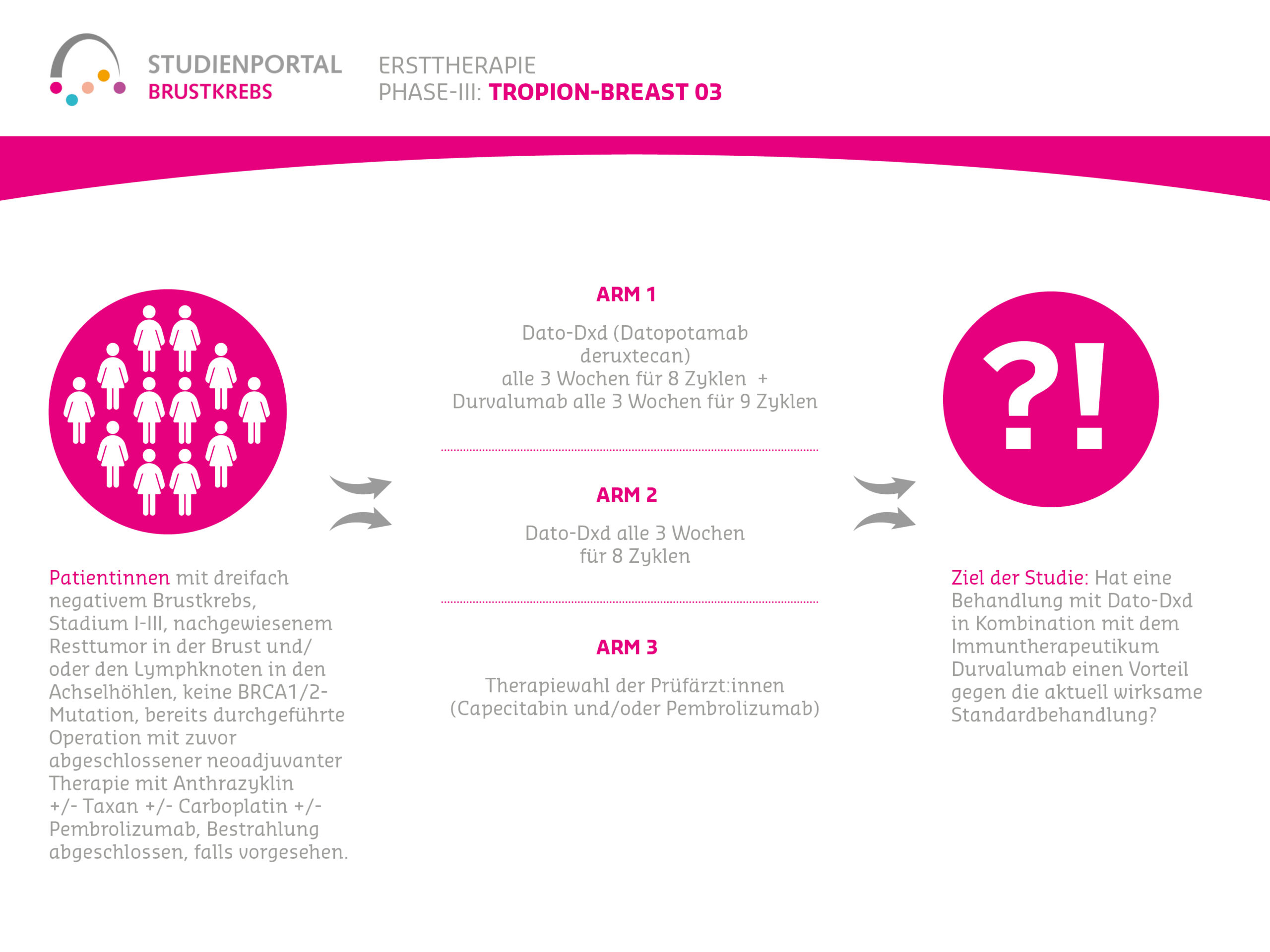
Im Rahmen der Studie gibt es drei Behandlungsmöglichkeiten („Arme“), denen die Patient:innen in einem Verhältnis von 2:1:2 zufällig zugeordnet werden:
Arm 1:
Datopotamab deruxtecan als intravenöse Infusion alle 3 Wochen für 8 Zyklen (Infusionen) zusammen mit Durvalumab intravenöse Injektion alle 3 Wochen für 9 Zyklen
Arm 2:
Datopotamab deruxtecan als intravenöse Infusion alle 3 Wochen für 8 Zyklen
Arm 3:
Aktuelle Therapie entsprechend der Leitlinien und nach Einschätzung der behandelnden Ärzte (Capecitabin und/oder Pembrolizumab)
Gibt es Risiken?
Über mögliche Risiken bzw. Nebenwirkungen, die mit der Teilnahme verbunden sind, werden Sie im Rahmen eines Aufklärungsgesprächs informiert.
Teilnahmevoraussetzungen
An dieser Studie können Männer und Frauen ab einem Alter von 18 Jahre teilnehmen, mit:
- dreifach negativem Brustkrebs, Stadium I-III
- Nachgewiesenem Resttumor in Brust oder den Lymphknoten in den Achselhöhlen
- Keine Mutation in den BRCA1/2 Genen (Nachweis in Blutzellen der Patient:in)
- Bereits durchgeführte Operation und zuvor abgeschlossene neoadjuvante Therapie mit Anthrazyklin +/- Taxan +/- Carboplatin +/- Pembrolizumab
- Bereits abgeschlossene Bestrahlung (falls vorgesehen)
Darüber hinaus gibt es aber auch noch weitere Kriterien, die für eine Teilnahme an der Studie erfüllt sein müssen. Interessierte Patientinnen sollten mit den Prüfärzt:innen an einem Studienzentrum sprechen, welche prüfen können, ob diese Studie für sie in Frage kommt.
Wo kann ich an dieser Studie teilnehmen?
Weitere Informationen zu teilnehmende Zentren finden Sie hier:
https://studienportal-brustkrebs.de/deutschlandkarte
Diese Studie wird unterstützt von: